Souvent associé à un grain de beauté qui dégénère, le cancer de la peau est en fait beaucoup plus complexe que cela. Pourtant, il existe des moyens simples de s’en protéger. Nous avons interrogé trois experts du sujet pour nous éclairer sur ce cancer cutané : le chercheur et Promoteur Télévie Cédric Blanpain, la dermatologue Laurence Walon et la dermatologue et membre du bureau de l’Euromelanoma Bernadette Blouard.
Quels sont les différents types de cancer de la peau ?
Il existe plusieurs types de cancers de la peau. Les trois plus fréquents s’appellent le carcinome basocellulaire, le carcinome épidermoïde et le tristement célèbre mélanome.
Le carcinome basocellulaire se présente sous la forme d’une tumeur sur la peau. Cédric Blanpain, chercheur et Promoteur Télévie, nous explique : « Le carcinome basocellulaire est de loin le cancer le plus fréquent chez l’Homme. On considère qu’environ une personne sur six ou une personne sur cinq (…) va développer un carcinome basocellulaire dans sa vie ». Détecté à un stade précoce, ce carcinome basocellulaire n’est pas grave dans la très grande majorité des cas car il ne donne pas de métastases. Celles-ci sont rapportées dans environ 0,1% des cas. Le traitement consiste en une simple opération, le dermatologue doit juste enlever la tumeur. Un bon traitement chirurgical est très important car un carcinome basocellulaire peut envahir la profondeur de la peau et récidiver.
Anciennement appelé carcinome spinocellulaire, le carcinome épidermoïde touche un million de personnes à travers le monde. Le Docteur Blouard, dermatologue et membre du bureau de l’Euromelanoma, explique « il se développe sur une lésion précancéreuse qui est bénigne mais qui peut dégénérer : la kératose actinique. » Celle-ci se présente sous forme de petite croûte qu’on retrouve sur les zones les plus exposées au soleil : le décolleté, le visage, le cuir chevelu,… Le carcinome épidermoïde peut donner des métastases dans 1% des cas. 99% des carcinomes épidermoïdes bénéficient d’un traitement local.
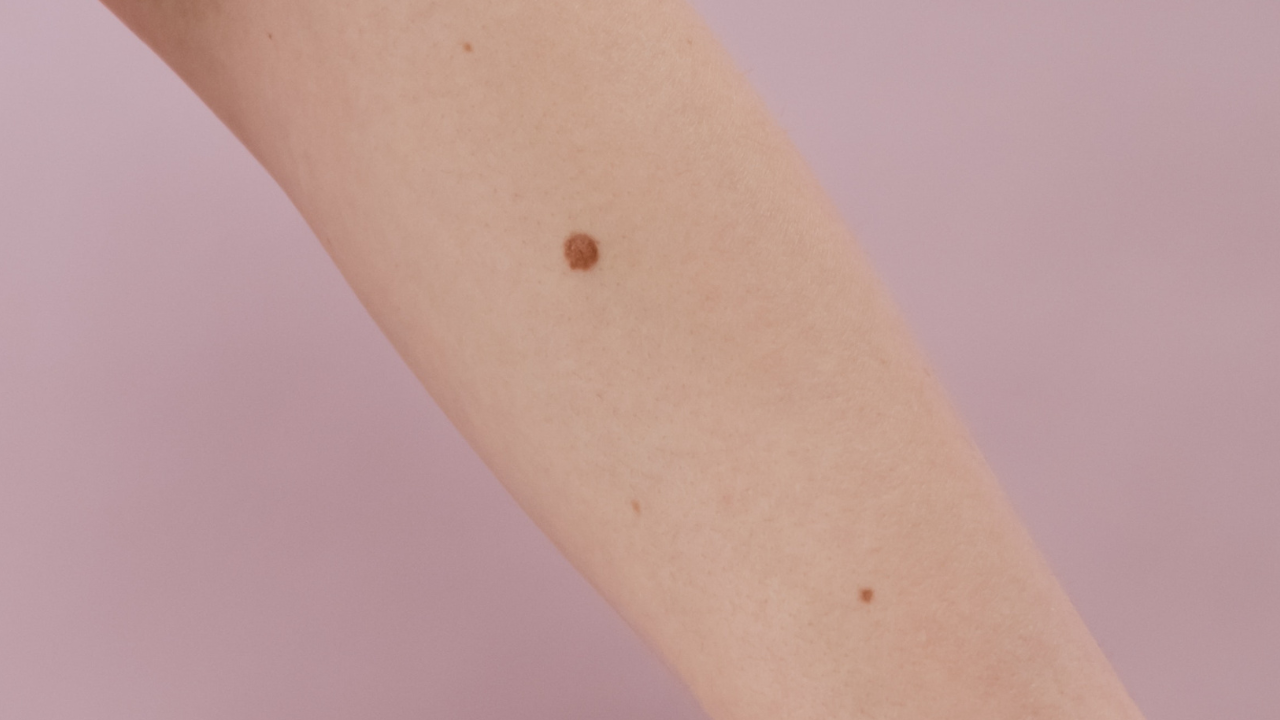
Mais le cancer de la peau le plus virulent et mortel reste le mélanome. Celui-ci provient des mélanocytes, des petites tâches que l’on a sur la peau. Peu importe leur taille, ces mélanomes peuvent donner des métastases très agressives. Un patient peut mourir de ce cancer dans les quelques mois ou quelques années après le diagnostic. Cédric Blanpain prévient « Il faut toujours être extrêmement vigilant avec les mélanomes (…) et ne pas attendre que la tumeur ait 2 cm de diamètre avant d’agir. » Le mélanome apparait dans 80% des cas sur une peau saine, il n’y a que dans 20% des cas qu’il est lié à un grain de beauté existant.
Le Registre du cancer rapporte qu’il y a chaque année plus de 70.000 nouveaux cas de cancers en Belgique. Il s’agit en fait de cancers potentiellement mortels. Parmi les cancers de la peau, seuls les mélanomes sont repris dans ces statistiques. Ceux-ci représentent 4% des cancers potentiellement mortels donc dont 90 % sont diagnostiqués au stade précoce. Le taux de survie à 5 ans est de plus de 90%. Même si une tumeur ou un cancer n’est pas potentiellement mortel, cela entraine une morbidité auprès des personnes concernées (anxiété, traitements chirurgicaux, complications rares,…). La prévention et le diagnostic précoce ont donc toute leur place et c’est d’autant plus vrai pour les mélanomes.
« Plus un cancer cutané est pris en charge tôt, plus on en guérit » Dr Walon
Comment développe-t-on un cancer de la peau ?
Selon le Docteur Walon, dermatologue, le cancer de la peau peut dépendre de l’âge mais également du capital UV entamé. Les dix premières années de vie sont les plus cruciales, elles peuvent déterminer un risque à long terme au niveau du cancer cutané. « Le risque le plus important, il est réalisé lors des dix premières années de vie d’un enfant d’exposition solaire ».
« Le soleil est un facteur stimulant extrêmement important mais qui n’est pas obligatoire. » En effet, comme l’explique le Dr Blouard, certaines personnes peuvent avoir un cancer de la peau sur des zones qui n’ont pas été exposées au soleil.
Quelles sont les personnes les plus à risque ?
Tous les scientifiques interrogés sont unanimes : les personnes avec des phototypes très clairs, les patients roux, blonds avec une peau claire sont des personnes à risque. Mais il n’y a pas qu’eux. Si vous souffrez du syndrome du naevus atypique, si vous avez des antécédents de cancer de la peau dans la famille, ou si vous avez vécu dans des pays ensoleillés étant enfant, vous avez également plus de risques de développer un cancer de la peau.
Comment détecter un cancer de la peau ?
Selon le Docteur Walon, dermatologue, l’auto-examen est un geste très important à avoir. « Il permet de détecter des lésions qui pourraient éventuellement se multiplier et changer. » Elle conseille à ses patients de se faire aider par un membre de leur famille pour les zones difficiles à inspecter. Il ne faut pas oublier les zones peu visibles : le dos, l’arrière des oreilles, le cuir chevelu, les zones génitales ou encore entre les orteils. En effet, les cancers de la peau peuvent se manifester à tous les endroits du corps, même ceux qui ne sont pas exposés au soleil car le soleil est un facteur responsable du cancer de la peau mais il n’est pas le seul. Si on détecte une lésion qui se serait modifiée ou une plaie qui ne guérit pas, il faut aller consulter un dermatologue.
Comment prévenir le cancer de la peau ?
Il ne faut pas s’exposer directement au soleil ou se mettre sur un transat pour accumuler des UV. 80% de notre exposition solaire provient de notre vie quotidienne : sortir, aller dans sa voiture, faire ses courses, … Le Docteur Blouard ajoute « Les pires vacances, c’est la Côte belge car il y a du vent et des nuages, on pense ne pas être exposé mais on l’est ». Pour se protéger de cette exposition silencieuse, il faut mettre de la crème solaire idéalement 365 jours par an sur les zones les plus exposées.
Au printemps ou en été, les dermatologues recommandent d’utiliser une crème solaire indice 50, de renouveler son application toutes les 2-3 heures et après chaque baignade. N’oubliez pas le dos des mains, le dos des pieds, les oreilles ou encore la nuque. Il faut également éviter de s’exposer aux heures chaudes, entre 12h et 16h. « Je conseille de porter un chapeau ou un bob plutôt qu’une casquette car la casquette ne couvre pas les oreilles », souligne le Docteur Blouard.
Est-ce que la recherche a aidé à faire avancer les traitements contre le cancer de la peau ?
En 30 ans, la recherche a énormément évolué. Des cancers de la peau qui étaient létaux à l’époque sont maintenant guérissables. Le carcinome basocellulaire, par exemple, peut être traité grâce à un traitement local d’immunothérapie. L’immunothérapie est aujourd’hui le traitement de choix pour les mélanomes métastatiques. La photothérapie dynamique permet de traiter certains carcinomes basocellulaires. Ce n’est pas parce que la recherche avance bien qu’on a trouvé la solution miracle pour sauver la peau. Le Professeur Blanpain et son équipe étudient tous les jours les cancers cutanés. « On comprend de mieux en mieux comment les cancers se développent, comment les cancers grandissent, comment les cancers se disséminent à distance. » La recherche sur les mélanomes reste indispensable car certains patients résistent à l’immunothérapie et aux médicaments ciblés. Quant aux recherches sur les carcinomes basocellulaires et les carcinomes épidermoïdes sont utiles pour la recherche fondamentale et pour servir de modèles pour les recherches sur d’autres types de cancers ou maladies.
« Le Télévie a un rôle capital dans le soutien à la recherche », Dr Blouard.
Quel est le futur du cancer de la peau ?
Les scientifiques s’attendent à voir le nombre de cancers de la peau augmenter dans les prochaines années. Pourquoi ? Car les personnes qui s’exposaient au soleil auparavant ne se protégeaient pas contre les rayons. Dans les années 60 ou 70, peu de personnes mettaient de la crème solaire. Selon le Dr Blouard, « le soleil est une bombe à retardement. » Heureusement, les campagnes de prévention commencent à porter leur fruit et tout le monde connait l’importance des gestes à avoir contre les effets négatifs du soleil. On s’attend donc à voir une baisse du nombre de cancers de la peau dû au soleil dans vingt ou trente ans.
Avec l’aimable collaboration scientifique du Professeur Jacques Boniver.