La thérapie par radioligands (RLT) et la radiothérapie sous apnée sont deux nouvelles thérapies qui ont fait l’actualité et qui ont le vent en poupe. Mais d’où viennent ces techniques ? Pourquoi en parle-t-on aujourd’hui ? Et surtout, que nous réservent-elles à l’avenir ?
Les réponses des Pr Xavier Geets, Chef de service de radiothérapie oncologique aux Cliniques Universitaires St-Luc (CUSL), et de son confrère, le Pr Renaud Lhommel, Chef de service de médecine nucléaire aux CUSL.
La radiothérapie sous apnée
Abordons d’abord peut-être la plus accessible de ces techniques, la radiothérapie sous apnée.
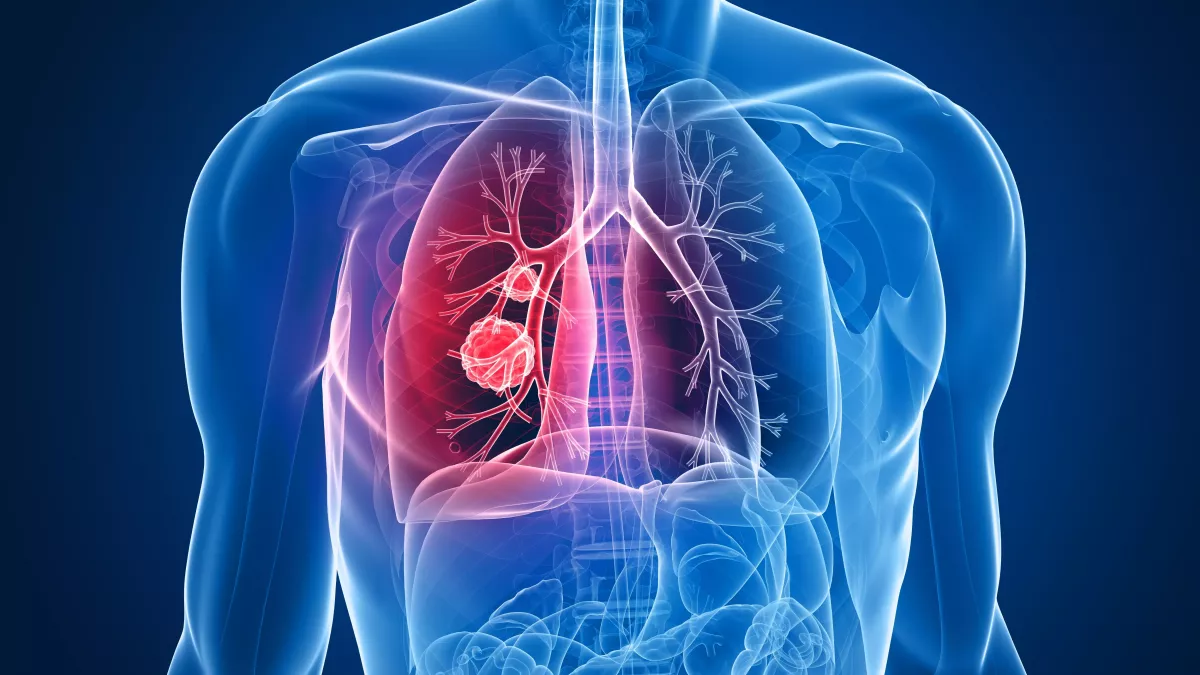
« Certaines tumeurs bougent et compliquent la radiothérapie. Les tumeurs du poumon, mais aussi du rein ou du foie, sont soumises au mouvement respiratoire. Or, la radiothérapie est une thérapie ciblée : il faut que les rayons arrivent au bon endroit », explique le Pr Xavier Geets.
Les radiothérapeutes avaient pris pour habitude d’irradier une zone plus large que la tumeur pour être certains de ne pas louper la cible. La conséquence ? Davantage de tissus sains sont irradiés, augmentant ainsi la toxicité du traitement. Certains se sont donc demandé : et si le patient ne respirait pas pendant l’irradiation ? « Cela rend la tumeur immobile et permet de limiter la région irradiée. »
Dans la plupart des centres, les traitements sont délivrés lorsque les patients font une inspiration bloquée volontaire. « Cela demande une participation active du patient. Or, ici, aux Cliniques Universitaires Saint-Luc (CUSL), c’est une machine qui induit cette inspiration bloquée. C’est un respirateur – une machine utilisée en anesthésie pour ventiler le patient endormi – qui a l’avantage de mieux réguler la respiration que l’humain. Cela permet de reproduire des apnées de façon stable et répétée d’une fois à l’autre. Et cela permet de tenir sur une plus longue durée sans respirer. »
Cela se fait sans sédation, en appliquant simplement un masque sur le patient, que l’équipe aura entraîné au préalable. « Il suffit de se laisser faire. Cela demande du lâcher-prise, mais c’est une démarche sécurisée puisque les machines sont dédiées à la respiration et permettent de monitorer le patient. »
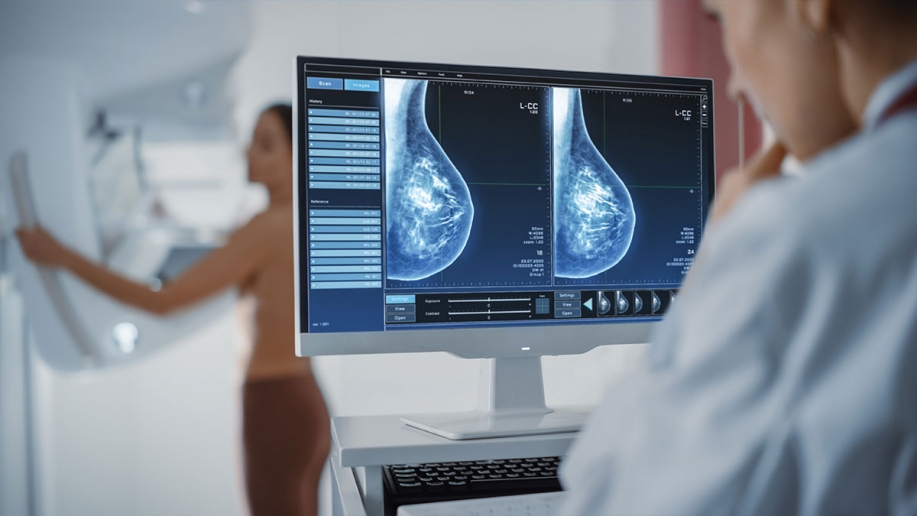
La technique est employée depuis plusieurs années aux CUSL et a démontré son efficacité pour le cancer du sein. Au-delà, elle ouvre la porte à d’autres applications en radiothérapie, comme le traitement du cancer du poumon, du foie, du rein ou des tumeurs de l’abdomen supérieur.
D’autres techniques existent, comme le tracking, où le faisceau irradiant suit en temps réel la position de la tumeur. Mais ces techniques sont plus complexes, coûtent cher et ne sont pas appropriées pour tous les patients. Or, tous les hôpitaux disposent de ventilateurs mécaniques qui leur permettent d’appliquer cette technique innovante à de nombreux patients. « Si l’on regarde un service de radiothérapie de plus près, on constate que quasiment la moitié des patients viennent pour des tumeurs mobiles. »
La thérapie par radioligands (RLT)
La RLT, en revanche, est plus difficile à comprendre.
« La RLT consiste à faire de la radiothérapie interne vectorisée. Si l’on identifie une cible cellulaire à la surface de cellules cancéreuses et qu’il existe une molécule connue, telle une protéine ou un anticorps spécifique, qui permet d’accéder et de se lier à la cible, il est possible d’ajouter un effet thérapeutique supplémentaire en fixant sur ce vecteur un isotope émetteur de particules bêta (électrons) ou alpha (noyau d’hélium), permettant d’irradier localement la cellule tumorale », explique le Pr Renaud Lhommel.
Il s’agit, plus simplement, d’une thérapie plus ciblée et, dès lors, plus efficace, qui comporte également assez peu d’effets secondaires grâce à un ciblage de plus en plus sélectif des tumeurs disséminées dans l’organisme. « Plusieurs études de phase 2 et de phase 3 démontrent aujourd’hui que la RLT ne présente pas de toxicité plus élevée que les stratégies thérapeutiques actuelles, ce qui pourrait à l’avenir éviter de recourir à des traitements plus délétères pour le patient, comme la chimiothérapie. »
Les effets bénéfiques de ce traitement ont d’abord été démontrés chez les patients qui étaient très loin dans leur maladie. C’est finalement une thérapie nouvelle, puisque des études pionnières concernant la RLT, telles que les études VISION et NETTER-1, n’ont été publiées dans le New England Journal of Medicine, une référence, qu’en 2017 et 2021. Cela a conduit au remboursement d’un médicament pour le cancer de la prostate en avril 2024.
Aujourd’hui, la RLT est utilisée pour traiter les tumeurs neuroendocrines – c’est par là que la thérapie par radioligands a commencé – et le cancer de la prostate métastatique.
Quel avenir pour ces deux technologies ?
« On a prouvé que l’on était capable de traiter des patients à des stades très avancés sans avoir de toxicité supplémentaire grâce à la RLT. Tout doucement, il y a une évolution de la stratégie thérapeutique pour proposer ce type de thérapies plus tôt dans la prise en charge, avant des thérapies plus délétères pour le patient, à l’instar des chimiothérapies », explique le Pr Lhommel.
D’autres cancers pourraient être ciblés par la RLT grâce aux molécules ciblées (HER2, FAPI…), comme le cancer du sein, les fibroblastes associés à certains cancers (tête et cou), ou encore les cancers du côlon, du pancréas ou du poumon. « Je pense que nous allons connaître des avancées significatives avec ce type de thérapies dans les prochaines années », confie le spécialiste.
L’avenir est également tout tracé pour la radiothérapie sous apnée. « L’objectif est de cibler davantage de cancers », explique le Pr Xavier Geets. « Le plus bel avenir de cette technique, c’est la radiothérapie adaptative, une radiothérapie où, à chaque séance, on peut observer l’anatomie du jour. Cela permet d’ajuster le traitement au mieux par rapport aux besoins du patient. C’est une étape clé vers une radiothérapie personnalisée, individualisée. »